TCDF investiga utilização de produto proibido para uso humano no Hmib
Unidade de saúde teria submetido paciente a itens vetados pela Agência Nacional de Vigilância Sanitária (Anvisa)
atualizado
Compartilhar notícia

O Tribunal de Contas do Distrito Federal (TCDF) investiga suposta utilização de “produto proibido para uso humano e fornecido por laboratório descredenciado pela vigilância sanitária” no Hospital Materno Infantil de Brasília (Hmib). A Corte apura também possível prejuízo aos cofres públicos e factíveis danos em pacientes após contato com os itens.
A Agência Nacional de Vigilância Sanitária (Anvisa) havia suspendido a fabricação, distribuição, comercialização e uso de 30 produtos da Vic Pharma Indústria e Comércio Ltda em 27 de abril de 2017, por meio de resolução. À época, o órgão regulador justificou que “foram constatadas desconformidades quanto às boas práticas de fabricação de medicamentos”.
A decisão da agência foi publicada em 2 de maio de 2018. De acordo com normas do órgão, o recolhimento dos produtos, nesses casos, deve ocorrer imediatamente.Os itens vetados são antissépticos essenciais para prevenção de infecções e realização de cirurgias, como álcool – inclusive o iodado –, usados em centros obstétricos, unidades de terapia intensiva (UTIs) e salas de curativos. Entre eles, estão também talco, óleo mineral, vaselina e bicarbonato de sódio.
Porém, segundo denúncia recebida pelo Ministério Público de Contas do Distrito Federal (MPC-DF), servidores e funcionários do Hmib mantiveram o uso dos itens, pelo menos, até 6 de maio. Ou seja, após a data em que os produtos deveriam ter sido recolhidos.
Confira lista de produtos da Vic Pharma proibidos pela Anvisa:

Também em 6 de maio, a Vigilância Sanitária do DF atestou o uso dos itens proibidos, segundo o MPC. Motivada por isso, a procuradora-geral de Contas Cláudia Fernanda de Oliveira Pereira representou contra a Secretaria de Saúde do Distrito Federal (SES-DF) no TCDF. O tribunal, então, cobrou explicações sobre a aquisição e os contratos referentes à Vic Pharma.
Neles, o Tribunal de Contas do Distrito Federal não encontrou irregularidades. Entretanto, para a corte, algumas questões não ficaram claras. Entre elas, a quantidade dos medicamentos referidos na resolução da Anvisa e dispensados entre 2 de maio e 14 de junho de 2017, por unidade de saúde. Além disso, o tribunal quer saber em quais pacientes os produtos foram utilizados e se houve relatos de intercorrências causadas por isso.
E mais: o TCDF questionou a SES-DF sobre “medidas administrativas adotadas para reparação do dano causado pelo recolhimento de medicamentos/insumos” provenientes da Vic Pharma e interditados pela Anvisa.
Decisão do TCDF by Metropoles on Scribd
“Da mesma forma, em relação às providências relativas à substituição/devolução dos valores pagos com os produtos impróprios pela fornecedora […] as informações prestadas pela SES foram incompletas, o que revela que, de qualquer forma, não haveria motivo de considerar totalmente atendida a determinação do Tribunal, como pontuou a Unidade Técnica”, manifestou o MPC junto ao TCDF.
Portanto, a Corte determinou 30 dias para a secretaria encaminhar as informações. A decisão consta da edição da terça-feira da semana passada (5/6) do Diário Oficial do Distrito Federal (DODF).
“A SES-DF comunicou ao tribunal as providências adotadas para retirar os produtos interditados da rede de saúde pública do Distrito Federal”, afirmou o TCDF ao Metrópoles.
“No entanto, não informou dados que demonstrem concretamente medidas adotadas atinentes às questões financeiras envoltas no fornecimento dos produtos, principalmente se a reparação do dano ao erário pela Vic Pharma foi devidamente equalizada”, acrescentou. Na prática, o TCDF quer saber se houve substituição sem custos dos medicamentos ou a compensação dos valores pagos.
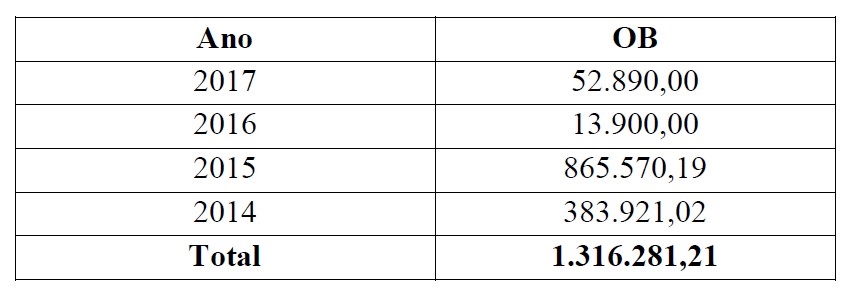
Veja as cifras pagas pelo governo do DF à empresa Vic Pharma, de acordo com o Sistema Integrado de Gestão Governamental (Siggo):
O que diz a SES-DF
A Secretaria de Saúde do Distrito Federal informou que comprou produtos da Vic Pharma antes da proibição emitida pela Anvisa. “Após o alerta, o Núcleo de Farmácia Hospitalar do Hmib recolheu todo o estoque do material”, acrescentou a pasta em nota enviada ao Metrópoles.