Governo Lula descumpre portaria e gasta R$ 457 milhões com Zolgensma
Ministério da Saúde atrasa distribuição do Zolgensma desde junho de 2023. Judicialização é o caminho encontrado para os pacientes
atualizado
Compartilhar notícia

O Ministério da Saúde gastou R$ 457 milhões com o fornecimento do Zolgensma – usado contra Atrofia Muscular Espinhal (AME) tipo I – em 2023 e 2024. Essa terapia gênica da Novartis deveria estar disponível no Sistema Único de Saúde (SUS) desde 4 de junho do ano passado, mas ainda não é ofertada aos pacientes. Uma das saídas encontradas para que não fiquem sem tratamento passa pela judicialização.
Ao todo, o governo federal desembolsou R$ 305 milhões em 2023, com 64 ações judiciais em 12 estados e no Distrito Federal. Mais R$ 152 milhões saíram dos cofres em 2024, com 41 processos em nove estados e na capital federal – recordista em casos judicializados.
A coluna obteve os dados a partir da Lei de Acesso à Informação (LAI). A resposta chegou na última quarta-feira (27/11).
O Instituto Nacional da Atrofia Muscular Espinhal (Iname) estima que haja 1.795 pacientes com AME no Brasil. Do total, 75 têm até 2 anos, idade limite para o uso do medicamento, de acordo com o aval da Agência Nacional de Vigilância Sanitária (Anvisa).
Das oito terapias gênicas aprovadas pela Anvisa, o maior gasto durante o governo de Luiz Inácio Lula da Silva (PT) se dá, disparadamente, com o Zolgensma (onasemnogeno abeparvoque). O valor acumulado dele é 44 vezes maior que o do segundo lugar: o Kymriah (tisagenlecleucel), para tratar alguns tipos de câncer de sangue, custou R$ 10,3 milhões ao governo – foram quatro processos neste ano.
Já o Luxturna (voretigeno neparvoveque), contra perda de visão causada por distrofia hereditária da retina, ocupa a terceira posição: foram R$ 4,6 milhões em um processo de 2023. Não houve judicialização dos outros cinco medicamentos no período.
O principal entrave para a disponibilização no SUS, apurou a coluna, é o preço que o governo arcará pelo Zolgensma, que ainda não está definido. Segundo interlocutores ligados ao tema, a pasta e a Novartis se reúnem nesta segunda-feira (2/12) para discutir ajustes no acordo de compartilhamento de risco (ACR). O último encontro foi em 22 de novembro.
“O maior desafio das pessoas com AME hoje é a equidade, ou seja, o acesso aos tratamentos para todos. Temos um medicamento que está incorporado, mas ainda não está disponível para as famílias: o Zolgensma. Temos, ainda, os pacientes do tipo III, que continuam sem acesso a tratamento. Essas duas questões precisam de solução urgente, pois quem tem uma doença degenerativa não pode esperar”, afirmou a diretora nacional do Iname, Diovana Loriato.
O que existe até o momento é um protocolo de intenções, assinado pelo ex-ministro da Saúde Marcelo Queiroga e pela Novartis em dezembro de 2022, às vésperas do fim do mandato. As diretrizes do SUS, de acordo com o anúncio oficial da época, definem que bebês com AME tipos I de até 6 meses e fora da ventilação invasiva por mais de 16 horas diárias podem ser contemplados.
À época, a justificativa dele para restringir a idade foi a maior eficácia do tratamento nessa faixa etária. Há famílias, porém, que judicializam o pedido da terapia gênica fora dos critérios estabelecidos pela pasta.
“Para que o medicamento seja disponibilizado à população, é necessária a atualização do Protocolo Clínico e Diretrizes Terapêuticas (PCDT) e a formalização de um Acordo de Compartilhamento de Risco (ACR), atualmente em fase de pactuação. Assim, o Ministério da Saúde oferece o medicamento Zolgensma apenas mediante ordem judicial, com a devida instrução da Advocacia-Geral da União”, informou a pasta em nota.
Diagnóstico de AME
Outra dificuldade passa pelo diagnóstico, que, muitas vezes, é de difícil acesso e precisa ser precoce para haver uma melhor evolução no tratamento.
“Se a criança não recebe (o Zolgensma), perde toda a possibilidade de ter uma melhora clínica, porque o problema da AME é que os neurônios que são perdidos não são recuperados. O que se espera é que não perca os neurônios. Por isso, a ideia é começar o quanto antes”, disse a geneticista e professora do Departamento de Genética e Biologia Evolutiva do Instituto de Biociências da Universidade de São Paulo (USP), Mayana Zatz.
A Lei 14.154/2021, que institui o teste do pezinho ampliado, tenta mudar esse cenário ao incluir a detecção da doença em recém-nascidos na quinta fase do exame. Essa legislação, porém, ainda não foi regulamentada. Distrito Federal e Minas Gerais são minoria ao oferecê-lo já com o diagnóstico de AME, uma vez que o avanço do Programa Nacional da Triagem Neonatal (PNTN), do Ministério da Saúde, é desigual no Brasil.
É responsabilidade da pasta comprar o Zolgensma, de forma centralizada com a fabricante. Segundo ofício enviado à coluna, o orçamento destinado a decisões judiciais está alocado conforme a Política ou o Programa de Saúde a que esteja ligado, em conjunto com a Subsecretaria de Planejamento e Orçamento (SPO). O do Zolgensma é vinculado à Secretaria de Ciência, Tecnologia e Inovação e ao Complexo Econômico-Industrial da Saúde (Sectics), comandada pelo economista Carlos Gadelha.
Associações se uniram para pressionar o governo pela liberação da terapia gênica. “Até que as famílias consigam o medicamento pela via judicial (o que pode demorar mais de 12 meses), os pacientes iniciam o tratamento com outro medicamento disponível no SUS. O custo, também elevado, desse tratamento ponte poderia ser evitado caso o Zolgensma estivesse disponível de imediato como primeira opção terapêutica”, diz manifesto do Universo Coletivo AME, obtido pela coluna.
Caminho do Zolgensma no SUS e nos planos de saúde
Um dos medicamentos mais caros do mundo, o Zolgensma entrou para o SUS em dezembro de 2022, após aval da Comissão Nacional de Incorporação de Tecnologias no SUS (Conitec). A partir de então, a Saúde tinha 180 dias para publicar o Protocolo de Tratamento e Diretrizes Terapêuticas (PCDT) – documento que norteia o cuidado com o paciente – e disponibilizar a terapia gênica.
O prazo, estipulado pela Lei 12.401/2011 e pelo decreto 7.646/2011, não se concretizou. A espera pelo Zolgensma soma quase 1 ano e 6 meses na rede pública até esta segunda-feira (2/12).
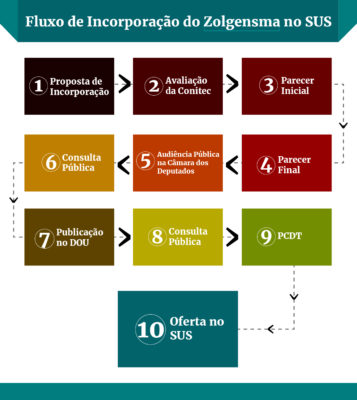
A decisão de incluí-lo no SUS não ocorreria se o parecer inicial, desfavorável à incorporação, fosse mantido. Veio, então, a consulta pública e a proposta da Novartis de fazer um acordo de compartilhamento de risco (ACR).
Esse último ponto mudou o rumo da decisão. Com a proposta na mesa, o ministério e a fabricante se propuseram a dividir a responsabilidade. Funciona da seguinte maneira, segundo o anúncio oficial: o pagamento deve se dividir em cinco parcelas anuais, de 20% do valor cada, condicionadas à evolução do paciente. Desse total, segundo a Novartis, 3% devem ser revertidos para o PNTN.
Dessa forma, a União não precisará arcar com os custos em caso de morte ou de piora. Os termos do acordo ainda estão em debate.
“A Novartis é contrária a judicialização como política de acesso a medicamentos, pois entendemos que isso prejudica a sustentabilidade do sistema e não garante o amplo acesso dos pacientes. Por isso, a companhia trabalha em estreita parceria e colaboração com os atores do sistema de saúde para viabilizar modelos customizados e sustentáveis de acesso. Dessa forma, todos os centros habilitados para o tratamento com ZOLGENSMA já possuem acordos comerciais estabelecidos e estão aptos a negociar os casos individualmente, caso necessário”, diz a nota.
Os requisitos do SUS também valem para os planos de saúde. O Zolgensma entrou para o rol da Agência Nacional de Saúde Suplementar (ANS) em fevereiro de 2023. Desde então, os planos de saúde são obrigados a custeá-lo, o que gerou uma discussão no setor.
O prazo das operadoras é menor que o da rede pública, uma vez que a Lei 14.307/2022 estabelece que os planos têm até 60 dias para incluir um tratamento recomendado pela Conitec e, posteriormente, incorporado pela Saúde.
O que é AME
A AME é uma doença genética rara, degenerativa, progressiva e hereditária que acomete células nervosas da medula espinhal e do cérebro. A causa reside numa mutação no gene SMN1, responsável pela produção da proteína SMN – a falta dela ocasiona na degeneração e na morte de neurônios motores, que controlam os movimentos musculares do corpo.
A doença se divide entre os tipos I (mais grave, afeta bebês), II (aparece em crianças de até 10 anos) e III (surge na adolescência e na vida adulta), explica Zatz, da USP. Estima-se que a AME acometa 1 em cada 10 mil pessoas. Além do Zolgensma, a Saúde já incorporou o nusinersena e o risdiplam como tratamentos.















